“Passé, avenir, pourquoi l'homme ne sait-il vraiment vivre que dans l'une ou dans l'autre, au mépris du présent ?” Michelle Le Normand
"Le temps est notre supplice. L'homme ne cherche qu'à y échapper, c'est-à-dire échapper au passé et à l'avenir en s'enfonçant dans le présent, ou se fabriquer un passé ou un avenir à sa guise.” Simone Weil
Analyse et décryptage par :

François Becker , Chamonix
MD, PhD, HDR, PU Médecine Vasculaire
Effect of atherosclerosis on 5-year risk of major vascular events in patients with transient ischaemic attack or minor ischaemic stroke: an international prospective cohort study, Effet de l'athérosclérose sur le risque à 5 ans d'événements vasculaires majeurs chez les patients victimes d'un accident ischémique transitoire ou d'un accident vasculaire cérébral ischémique mineur : une étude de cohorte prospective internationale
Lavallée PC, Charles H, Albers GW, Caplan LR, Donnan GA, Ferro JM, Hennerici MG, Labreuche J, Molina C, Rothwell PM, Steg PG, Touboul PJ, Uchiyama S, Vicaut É, Wong LKS, Amarenco P; TIAregistry.org Investigators. Lancet Neurology 2023 Apr; 22(4): 320-29 https://www.thelancet.com/journals/laneur/article/PIIS1474-4422(23)00067-4/abstract
Lavallée PC, Charles H, Albers GW, Caplan LR, Donnan GA, Ferro JM, Hennerici MG, Labreuche J, Molina C, Rothwell PM, Steg PG, Touboul PJ, Uchiyama S, Vicaut É, Wong LKS, Amarenco P; TIAregistry.org Investigators. Lancet Neurology 2023 Apr; 22(4): 320-29 https://www.thelancet.com/journals/laneur/article/PIIS1474-4422(23)00067-4/abstract
L’histoire des Accidents Ischémiques Transitoires (AIT) est intéressante, instructive (1-4).
L’introduction de la Coumadine en thérapeutique aux USA a bouleversé la prise en charge des affections vasculaires cérébrales aigues et a conduit à la tenue de conférences visant à classifier la pathologie vasculaire cérébrale et à envisager des essais cliniques en la matière (Princeton Conferences, 1 ère en 1954 sous l’égide de l’AHA). Lors de la 2 ème conférence, publiée en 1958, C.M. Fisher a fait une présentation originale intitulée « Intermittent Cerebral Ischemia », on a retenu le terme de « transient ischemic attacks » et oublié la durée du déficit « may last from a few seconds up to several hours, the most common duration being a few seconds up to 5 or 10 minutes ». L’AIT n’entrera dans la classification des affections cérébro-vasculaires qu’en 1975 (5). A ce stade on peut faire plusieurs remarques
* Détail mais quand même, le sigle qui est passé en pratique est celui de TIA ou d’AIT sans préciser le territoire concerné … (on parle rarement d’ischémie cérébrale transitoire).
* Le document officiel de 1975 a retenu une durée maximale du déficit de 24h sans que l’on sache exactement d’où vient ce délai de 24h (probablement lié aux propos d’un anglais, J. Marshall).
* En 1975, il n’y avait pas d’imagerie cérébrale disponible en pratique clinique.
* Le déficit doit avoir totalement régressé mais ce n’est pas toujours dit clairement et on peut confondre régression totale et réduction de la symptomatologie avec persistance d’un déficit mineur.
* Le plus grave est que l’AIT a été souvent présenté comme un accident mineur sans gravité méconnaissant le risque de récidive sous forme d’AVC ischémique constitué.
* Détail mais quand même, le sigle qui est passé en pratique est celui de TIA ou d’AIT sans préciser le territoire concerné … (on parle rarement d’ischémie cérébrale transitoire).
* Le document officiel de 1975 a retenu une durée maximale du déficit de 24h sans que l’on sache exactement d’où vient ce délai de 24h (probablement lié aux propos d’un anglais, J. Marshall).
* En 1975, il n’y avait pas d’imagerie cérébrale disponible en pratique clinique.
* Le déficit doit avoir totalement régressé mais ce n’est pas toujours dit clairement et on peut confondre régression totale et réduction de la symptomatologie avec persistance d’un déficit mineur.
* Le plus grave est que l’AIT a été souvent présenté comme un accident mineur sans gravité méconnaissant le risque de récidive sous forme d’AVC ischémique constitué.
L’introduction du scanner cérébral puis de l’IRM cérébrale et la réalisation d’études de suivi
des patients ayant fait un AIT ont changé la donne. La pratique de l’imagerie cérébrale a conduit à changer la définition d’un AIT. Les études de suivi ont montré que l’AIT est un puissant marqueur de risque d’AVC ischémique constitué à court terme. Le tout implique que le patient victime d’un AIT doit être pris en charge en urgence.
* Définition « actuelle » (2009) d’un AIT : Episode transitoire de troubles neurologiques en rapport avec une ischémie focale cérébrale, médullaire ou rétinienne, sans infarctus aigu$ (6). En fait les progrès de l’imagerie notamment IRM montrent que l’on trouve toujours des lésions tissulaires
la définition de 2009 ne semble plus valable (7). La tendance actuelle est de grouper TIA et Minor ischaemic stroke. Même si de vraies attaques ischémiques transitoires sans lésions tissulaires existent malgré une évaluation idéale,
l'utilité de distinguer un AIT d'un AVC mineur reste peu claire. Les deux présentent un risque élevé d'ischémie cérébrale ultérieur, répondent tous deux à des traitements similaires et peuvent avoir des effets similaires sur le patient.
* Risque d’AVC ischémique constitué à court terme : 3 à 10% à 7 jours, 4 à 20% à 3 mois selon les études et leur ancienneté. Environ 50% des AVC ischémique constitué surviennent dans les 48h après un AIT (8)
* Risque d’AVC ischémique constitué à moyen et long terme : 5,9 % dans un délai d’un an, de 12,8 % dans un délai de 5 ans et de 19,8 % dans un délai de 10 ans (Cf Blog MedVasc du 29/03/25).
* Risque d’AVC ischémique constitué à court terme : 3 à 10% à 7 jours, 4 à 20% à 3 mois selon les études et leur ancienneté. Environ 50% des AVC ischémique constitué surviennent dans les 48h après un AIT (8)
* Risque d’AVC ischémique constitué à moyen et long terme : 5,9 % dans un délai d’un an, de 12,8 % dans un délai de 5 ans et de 19,8 % dans un délai de 10 ans (Cf Blog MedVasc du 29/03/25).
Le travail qui fait l’objet de ce billet cible un autre point, le risque attribuable aux AIT et AVCi mineurs est-il le même quelle que soit leur étiologie ou varie-t-il en fonction de l’étiologie. Il est suffisamment important pour avoir fait l’objet de 2 articles dans des revues de 1 er plan, l’un dans le Lancet Neurology (2023 Apr) référencé ci-dessus, l’autre dans le JAMA Neurology (2023 Nov. - 9).
Les auteurs ont utilisé la codification ASCOD pour estimer le risque d’accident vasculaire majeur à 5 ans après un AIT dans un registre international, prospectif observationnel de patients ayant présenté récemment un AIT ou un AVC ischémique mineur (Echelle de Rankin modifiée 0-1). Ce registre international est le fait de 61 centres spécialisés dans 21 pays d’Europe, d’Asie, du Moyen Orient, d’Amérique latine. 4789 patients y ont été inclus du 1er juin 2009 au 29 décembre 2011, 3847 patients de 42 centres ont été inclus dans l’étude de suivi 5 ans (1, 3, 12 mois puis tous les ans), 3383 (88%) ont eu une visite à 5 ans. Le critère principal de jugement était un critère composite : AVC non-fatal (ischémique ou hémorragique, durée du déficit de24h), Accident coronarien aigu non-fatal (infarctus du myocarde ou angor instable) ou décès de cause cardio-vasculaire dans les 5 ans.

Codification ASCOD (10)
A : Athérosclérose (Atherosclerosis)
S : Maladie des petites artères (Small vessel disease)
C : Maladie cardiaque (Cardiac pathology)
O : Autre cause (Other causes)
D : Dissection (Dissection)
ASCOD Grade, degré de probabilité
1 : La maladie artérielle est présente et potentiellement causale.
A1 : Athérosclérose avec sténose ≥ 50% extra ou intracrânienne ipsilatérale à la zone
d’ischémie cérébrale ou thrombus (mobile) de l’arche aortique
2 : La maladie artérielle est présente mais le lien causal est incertain.
A2 : Athérosclérose avec plaque 30-50% extra ou intracrânienne ipsilatérale à la zone
d’ischémie cérébrale ou plaque d’épaisseur de 4 mm de l’arche aortique sans thrombus.
3 : La maladie artérielle est présente mais le lien causal est peu probable.
A3 : Plaque d’athérosclérose de 30% ipsilatérale à la zone d’ischémie cérébrale ou plaque
/sténose sur une artère cérébrale n’alimentant pas la zone d’ischémie cérébrale ou plaque d’épaisseur de 4 mm sur l’arche aortique sans thrombus ou athérosclérose coronaire ou membres inférieurs connue.
A3 : Plaque d’athérosclérose de 30% ipsilatérale à la zone d’ischémie cérébrale ou plaque
/sténose sur une artère cérébrale n’alimentant pas la zone d’ischémie cérébrale ou plaque d’épaisseur de 4 mm sur l’arche aortique sans thrombus ou athérosclérose coronaire ou membres inférieurs connue.
0 : la maladie artérielle est absente.
A0 : Pas d’athérosclérose documentée.
9 : bilan incomplet pour chaque catégorie,
A9 : N’a pas été investigué pour athérosclérose
Résultats.
Sur les 3847 patients inclus :
1406 (37%) étaient ASCOD A0 (AIT non lié à une lésion d’athérosclérose),
- 998 (26%) étaient ASCOD A1 (AIT très probablement lié à une lésion d’athérosclérose) ou A2 (lésion d’athérosclérose présente mais lien causal incertain),
- 1108 (29%) étaient ASCOD A3 (athérosclérose présente mais sans lien direct avec la zone d’ischémie cérébral) et
335 (9%) ASCOD A9 (pas d’investigation à la recherche de lésions d’athérosclérose).- Taux à 5 ans d’événements vérifiant le critère principal de jugement
- Patients ASCOD A0 : 7·7% (95% CI : 6·3–9·2; 101 événements)
- Patients ASCOD A1 ou A2 : 19·8% (95% IC 17·4–22·4; 189 événements). HR 2.77 (95%IC : 2.18-3.53, p 0.0001) par rapport aux patients ASCOD A0.- Patients ASCOD A3 : 13·8% (95%IC : 11·8–16·0; 144 événements). HR 1.87 (95%IC 1.45- 2.42, p< 0.0001) par rapport aux patients ASCOD A0.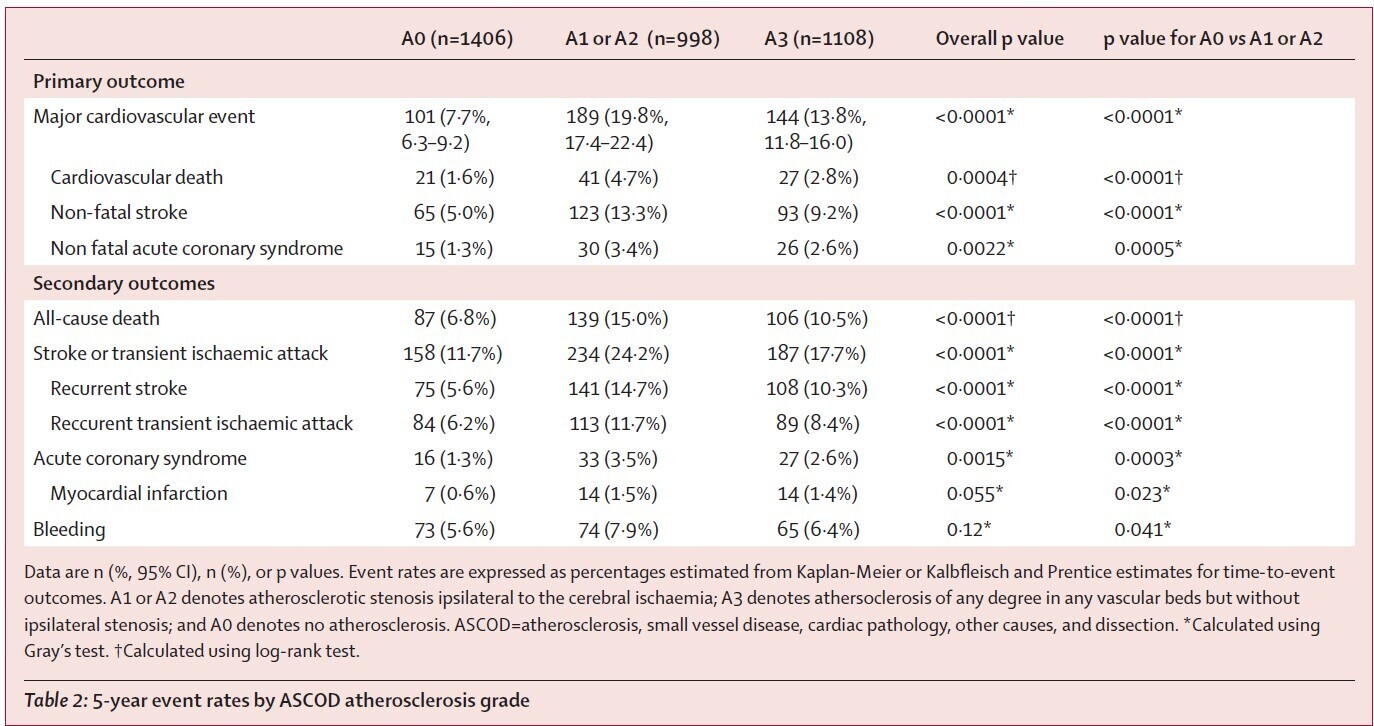
A noter que ce taux d’événements dans les groupes ASCOD A1 et A2 survient malgré les traitements prescrits : Anti-HTA (78%), Statines (72%), Hypoglycémiants (22%), Anti- agrégants plaquettaires (77%) ou Anticoagulants (15%).
En dehors de l’âge, du sexe masculin et d’infarctus multiples à l’imagerie cérébrale, la plupart des facteurs de risque identifiés dans les groupes A1 et A2 étaient des facteurs de risque modifiables (HTA, dyslipidémie, obésité, tabagisme, faible niveau d’activité physique).
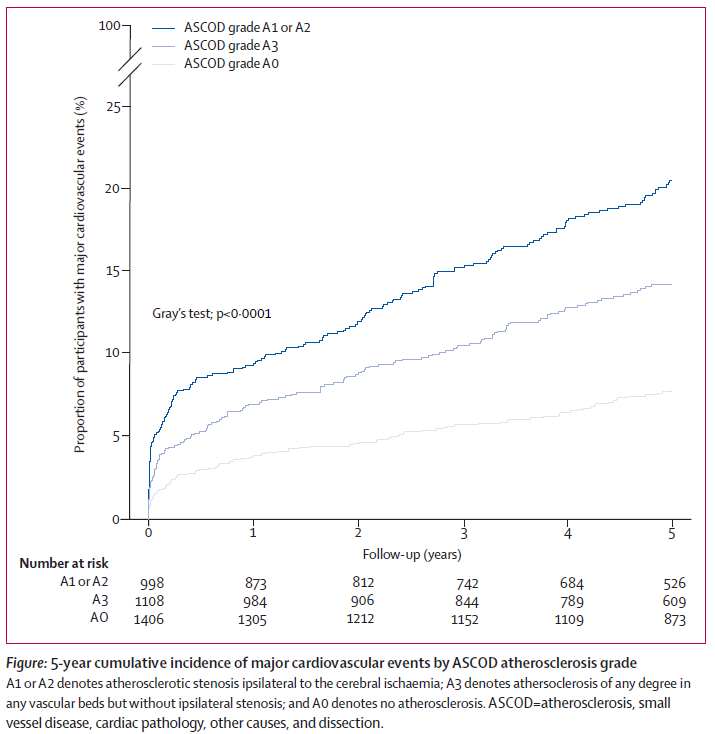
Le graphique ci-dessous illustre par ailleurs le fait que le risque d’événements cardio- vasculaire majeur après un AIT ou un AVCi mineur est certes élevé dans les premières semaines suivant l’AIT ou l’AVCi mineur mais que l’augmentation du risque se poursuit régulièrement durant les mois et années suivant.
Conclusion logique :
Les patients victimes d’un AIT ou d’un AVC ischémique mineur forment un groupe hétérogène. Les patients atteints d'athérosclérose présentent un risque beaucoup plus élevé d' événements cardio-vasculaires majeurs dans les 5 ans que les patients non atteints d'athérosclérose. Les stratégies préventives visant à traiter les complications d'athérosclérose devraient se concentrer sur les personnes atteintes d'athérosclérose plutôt que de regrouper toutes les personnes ayant subi un AIT ou un AVC ischémique mineur (y compris celles non atteintes d'athérosclérose).
Les AIT et AVC ischémiques mineurs liés à des lésions d’athérosclérose sont à haut risque d’événements cardio-vasculaires majeurs non seulement dans les jours et semaines qui suivent l’accident initial mais à long terme (au moins dans les 5 ans). Ils nécessitent une prévention secondaire au top.
On est très loin de la réputation de bénignité qui avaient été attribuée aux AITs par le passé !
Références
1. Fisher C.M. Transient Ischemic Attacks. New Engl J Med 2002 Nov 21
2. Easton J.D.. Redifining TIA. Neurology 2004 Apr
3. Mohr J.P.. Historical perspective. Neurology 2004 Apr
4. RPC. Prise en charge diagnostique et traitement immédiat de l’accident ischémique transitoire de l’adulte. Argumentaire. ANAES 2004 Mai
5. National Institute of Neurological Disorders and Stroke. A classification and outline of
cerebrovascular diseases. II. Stroke 1975;6(5):564-616
6. Easton J.D., Saver J.L., Albers G.W. et al Definition and evaluation of Transient Ischemic Attack. AHA, ASA Council. Stroke 2009 May
7. Easton J.D., Johnston S.C. Time to retire the concept of Transient Ischemic Attacks. JAMA 2022 March
8. Lamme J., Sauvin M., Sztajzel R. Prise en charge de l’accident ischémique transitoire. Rev Med Suisse 2022 ; 18 :1671-6
9. Lavallée PC, Charles H, Albers GW, Caplan LR, Donnan GA, Ferro JM, Hennerici MG, Labreuche J, Molina C, Rothwell PM, Steg PG, Touboul PJ, Uchiyama S, Vicaut É, Wong LKS, Amarenco P; TIAregistry.org Investigators. Underlying Causes of TIA and Minor Ischemic Stroke and Risk of Major Vascular Events. JAMA Neurol 2023 Nov 1;80(11):1199-1208.
10. Amarenco P, Bogousslavsky J, Caplan LR et al. The ASCOD phenotyping of ischemic stroke (Updated ASCO Phenotyping). Cerebrovascular Diseases 2013; 36: 1–5.
F. Becker 05/04/25
Merci François pour cette analyse "as usual", précise, didactique et parfaite
Copyright : Dr Jean Pierre Laroche / 2025

