- "Les machines seront peut-être capables un jour de penser, mais elles seront toujours incapables de rêver. " Walter Lippmann, écrivain, journaliste, intellectuel
- "Les robots intelligents sont la prochaine étape de l’évolution humaine" David Hanson, roboticien, fondateur de Hanson Robotics
" L’intelligence artificielle est tout ce qui n’a pas encore été fait." Larry Tesler,
"La connaissance sans la sagesse, est de l'intelligence artificielle...." Juliana M. Pavelka
https://www.cell.com/cell/fulltext/S0092-8674(25)01498-9
Article en libre accès

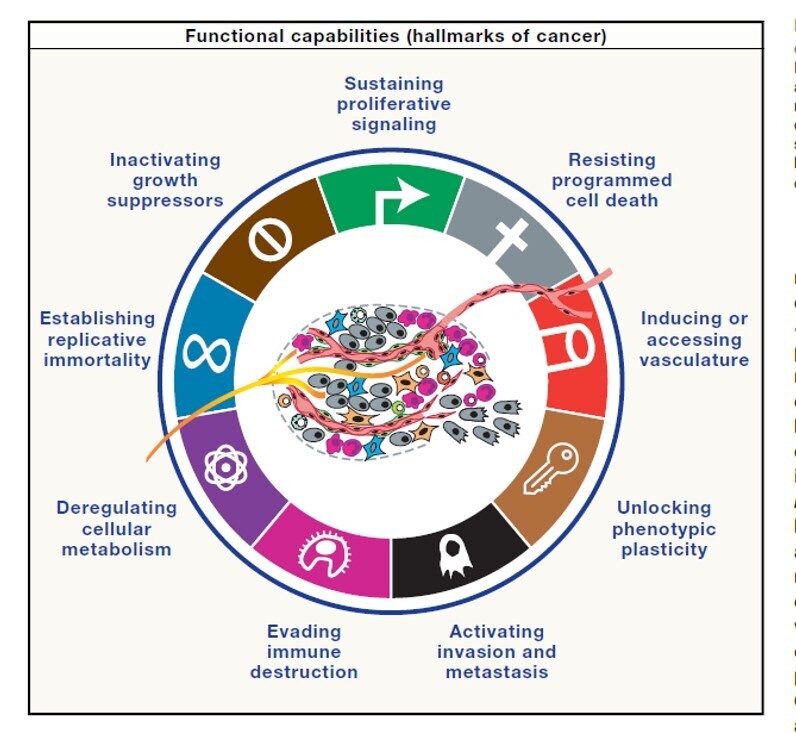
Les caractéristiques du cancer : Capacités fonctionnelles acquises
Dans le synopsis actuel, neuf capacités distinctes sont acquises de diverses manières à différents stades du développement tumoral multistapes et de l'évolution de formes spécifiques de cancer. Leur acquisition n'est pas strictement linéaire, et la dépendance à l'égard de certaines capacités peut être moindre que pour d'autres, voire inexistante, au cours de voies de tumorigenèse particulières.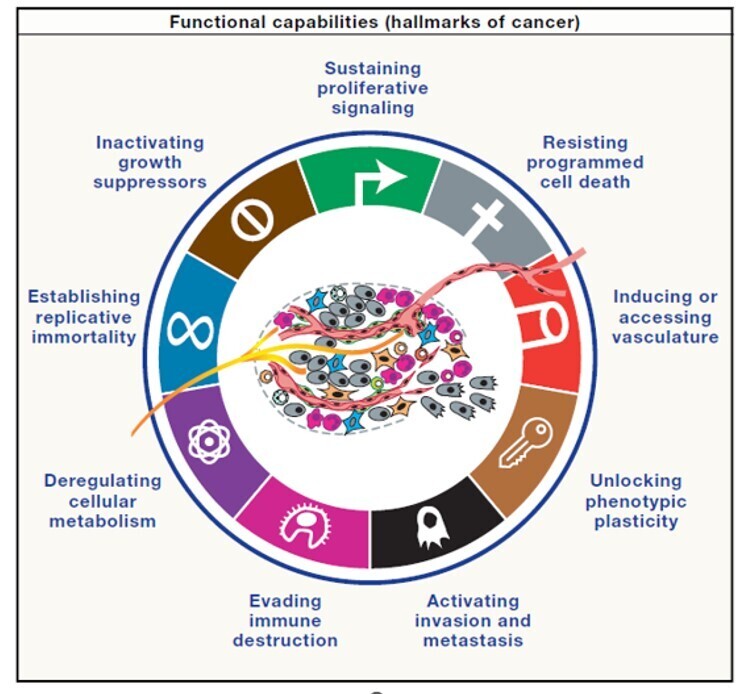
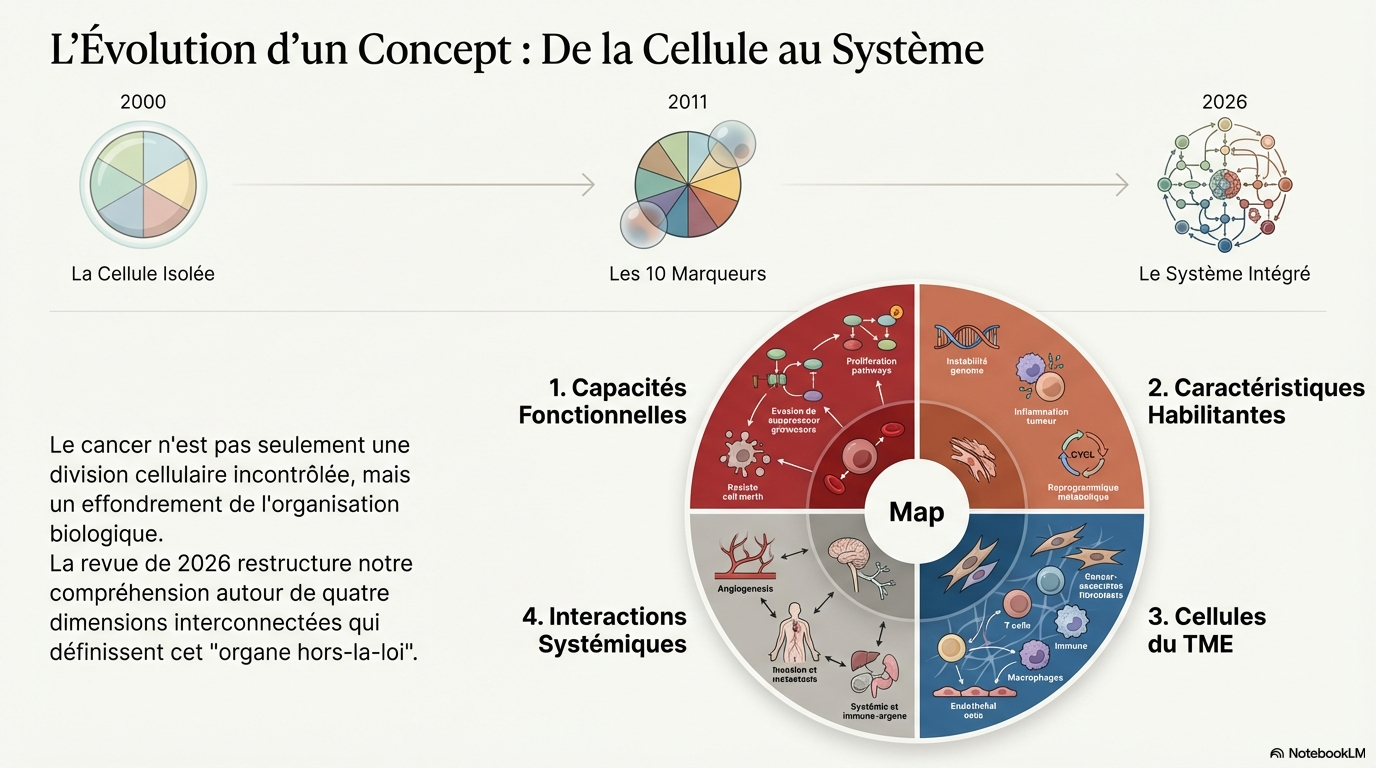
Les dimensions du cancer
Quatre dimensions conceptuelles distinctes fournissent une base logique pour condenser la complexité du cancer en composantes mécanistiques qui, collectivement, décrivent l'essence même de la maladie. Les paramètres opérant dans chaque dimension sont définis tout au long de cette revue.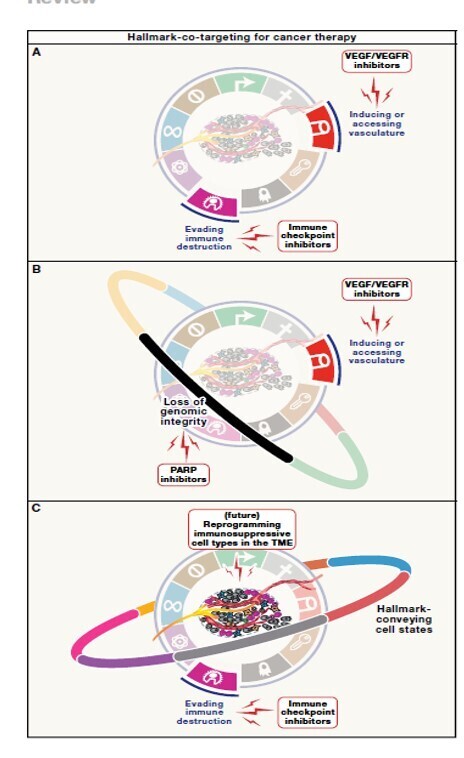
Justification du co-ciblage thérapeutique des caractéristiques du cancer
Il est de plus en plus évident que les futures améliorations des traitements contre le cancer proviendront en grande partie de combinaisons médicamenteuses de plus en plus sophistiquées, visant à la fois à accroître l'efficacité et à contourner les mécanismes de résistance intrinsèques et adaptatifs propres à la plupart des monothérapies. Les concepts résumés dans cette revue suggèrent une stratégie thérapeutique reposant sur le co-ciblage de différentes caractéristiques du cancer, ainsi que des paramètres associés à ces caractéristiques dans les autres dimensions conceptuelles, à l'aide de médicaments guidés par le mécanisme d'action. On peut envisager que l'induction d'une résistance adaptative concomitante à des cibles thérapeutiques mécanistiquement indépendantes s'avérera difficile pour les cancers co-ciblés, prolongeant ainsi l'efficacité et retardant la rechute.
(A et B) Exemples de co-ciblages thérapeutiques de caractéristiques cliniquement approuvés — « lueurs d'espoir » (signs of light) — qui encouragent la poursuite de l'évaluation de cette logique.
(C) Un exemple, encore non réalisé, d'une stratégie thérapeutique impliquant des inhibiteurs de points de contrôle immunitaire (ICI) combinés à des médicaments perturbant les mécanismes (ou cellules) effecteurs opérant dans le microenvironnement tumoral immunosuppresseur
Ce document traite de l'évolution des "hallmarks" du cancer, en présentant une synthèse des capacités fonctionnelles acquises et des caractéristiques phénotypiques qui définissent la biologie du cancer.
Les hallmarks du cancer : évolution et Perspectives
Cette revue présente une synthèse des hallmarks du cancer, soulignant leur évolution et leur pertinence pour développer nouvelles stratégies thérapeutiques.
Les hallmarks du cancer : capacités fonctionnelles acquises
- * Les hallmarks du cancer incluent neuf capacités fonctionnelles acquises au cours de la tumorigenèse.
- * Ces capacités ne sont pas strictement linéaires et varient selon les types de cancer.
- * Les capacités comprennent :
- - Maintien de la signalisation proliférative
- - Inactivation des suppressors de croissance
- - Résistance à la mort cellulaire programmée
- - Établissement de l'immortalité réplicative
- - Induction ou accès à la vascularisation
- - Activation de l'invasion et de la métastase.
- - Dérégulation du métabolisme cellulaire
- - Évasion de la destruction immunitaire.
- - Déverrouillage de la plasticité phénotypique
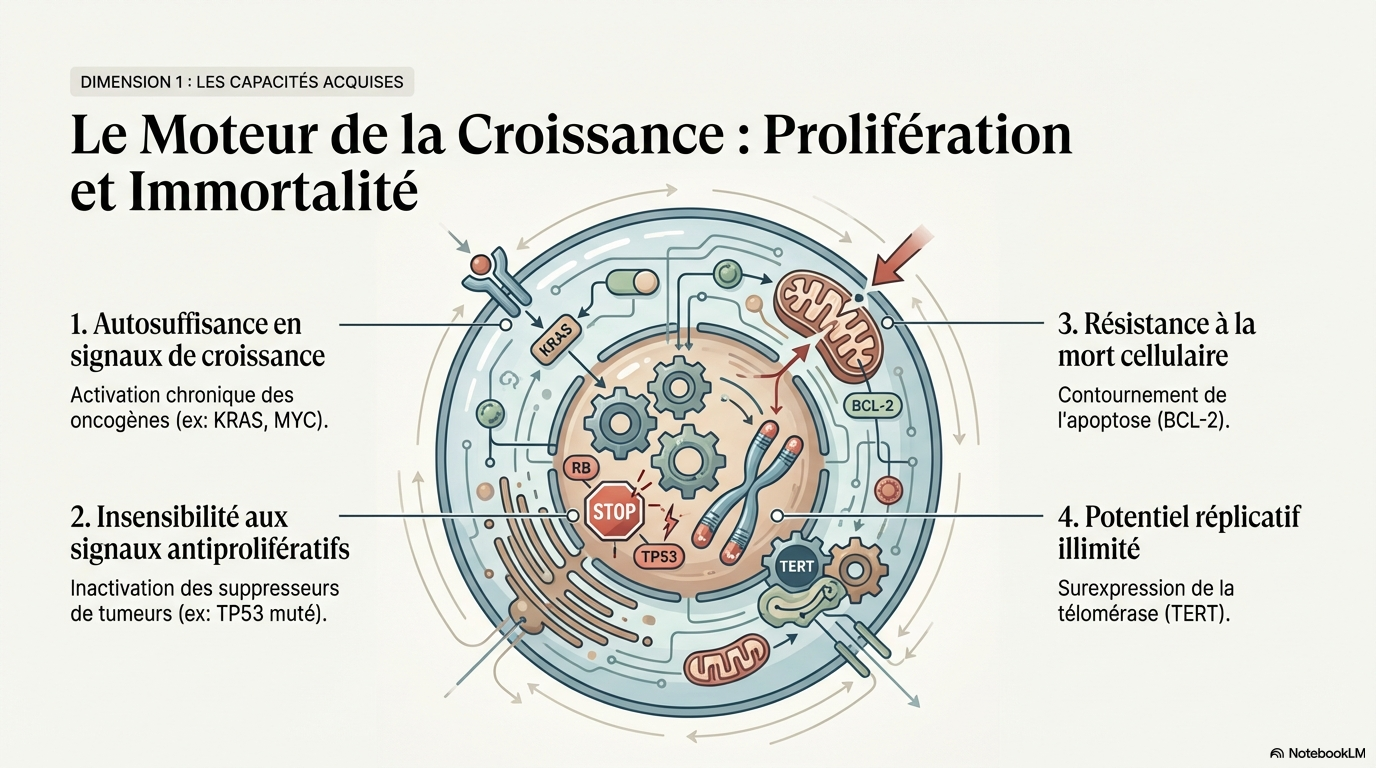
Maintien de la signalisation proliférative
- * La signalisation proliférative est essentielle pour la croissance des cellules cancéreuses.
- * Environ 30% des tumeurs humaines présentent des mutations activatrices dans le gène KRAS.
- * D'autres oncogènes comme PIK3CA et BRAF sont également impliqués.
- * 193 gènes ont été identifiés comme oncogènes de prolifération dans la base de données COSMIC
Inactivation des suppresseurs de croissance
- * Les gènes suppresseurs de tumeurs (TSGs) sont souvent inactivés dans les cancers.
- * Les mutations dans TP53, un TSG clé, sont présentes dans environ 40% des cancers.
- * 143 gènes ont été identifiés comme suppresseurs de croissance dans les tumeurs humaines.
Résistance à la mort cellulaire programmée
- * La résistance à l'apoptose est une caractéristique clé des cellules cancéreuses.
- * Les protéines anti-apoptotiques comme BCL-2 sont souvent surexprimées dans les cancers.
- * Des médicaments comme le venetoclax ciblent ces mécanismes pour traiter certains cancers.
Établissement de l'immortalité réplicative
- * Les cellules cancéreuses contournent le mécanisme de vieillissement cellulaire lié aux télomères.
- * Environ 15% des tumeurs humaines présentent des mutations dans le promoteur du gène TERT.
- * L'activation de TERT ou l'allongement alternatif des télomères (ALT) permet une prolifération continue.
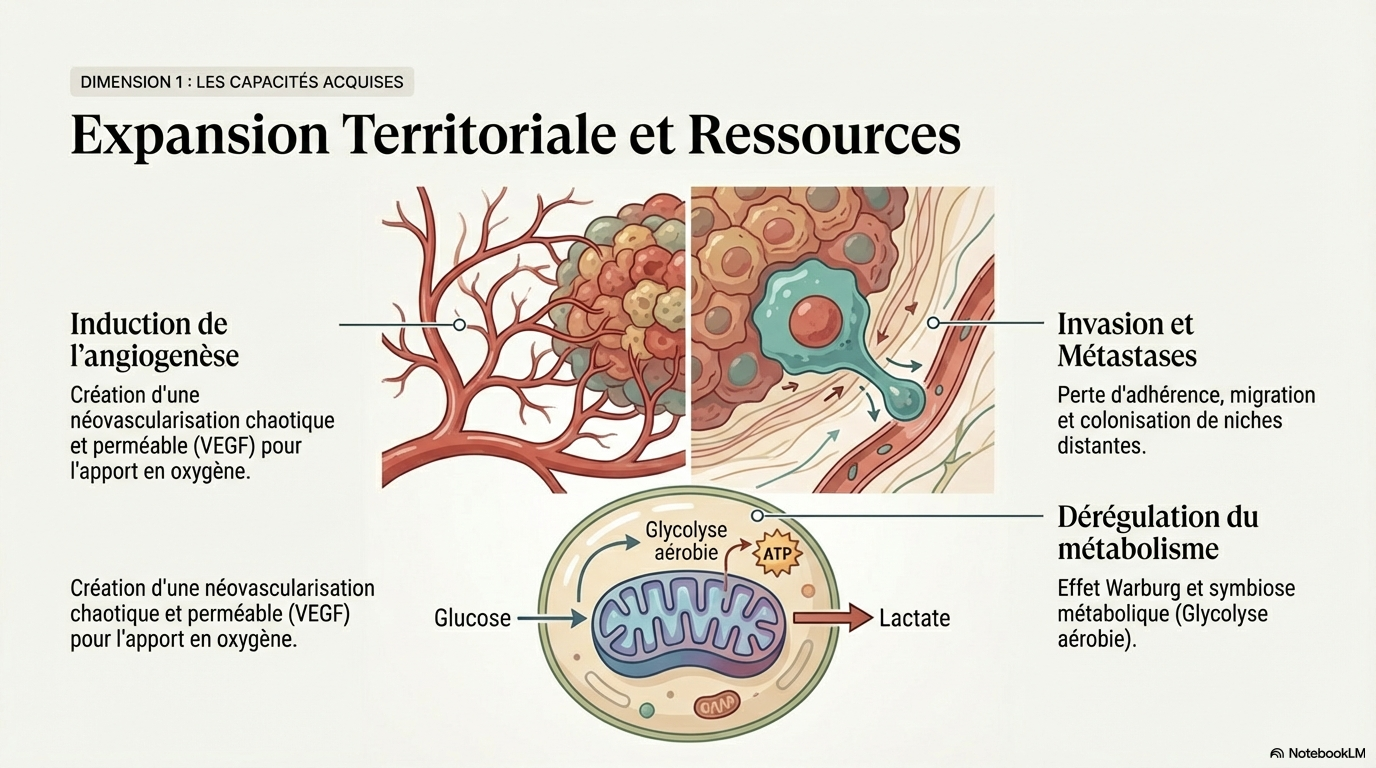
Induction ou Accès à la vascularisation
- * La vascularisation est cruciale pour fournir oxygène et nutriments aux cellules cancéreuses.
- * Les tumeurs peuvent induire l'angiogenèse via des facteurs de croissance comme VEGFA.
- * La co-option vasculaire permet également aux tumeurs de croître sans angiogenèse.
Dérégulation du Métabolisme Cellulaire
- * Les cellules cancéreuses adoptent des phénotypes métaboliques hybrides pour soutenir leur croissance.
- * Elles utilisent à la fois la phosphorylation oxydative et la glycolyse aérobie.
- * Les facteurs extrinsèques du microenvironnement tumoral influencent la programmation métabolique.
Déverrouillage de la plasticité phénotypique
- * La plasticité phénotypique permet aux cellules cancéreuses de s'adapter et de résister aux traitements.
- * Deux classes de plasticité : intra-lignée et trans-lignée, facilitent la diversité cellulaire.
- * La perte de TP53 favorise la dé-différenciation et la plasticité des cellules cancéreuses.
Évasion de la destruction immunitaire
Les cancers acquièrent la capacité d'échapper à la destruction immunitaire en supprimant les systèmes immunitaires adaptatifs et certains composants de l'immunité innée.
- * Les cellules tumorales exploitent la programmation innée des cellules T et NK pour éviter une activation chronique.
- * L'activation des cellules T entraîne un état d'épuisement, limitant la destruction des tumeurs.
- * Les mécanismes d'immunosuppression dans le microenvironnement tumoral (TME) varient selon le type de tumeur et le stade de la tumorigenèse.
- * Les cellules immunitaires, y compris les macrophages et les cellules endothéliales, contribuent à l'immunosuppression.
- * Les facteurs chimiques et physiques du TME, comme l'hypoxie et la composition de la matrice extracellulaire, inhibent les réponses immunitaires.
Activation de l'invasion et de la métastase
L'invasion et la métastase sont des processus complexes qui augmentent la morbidité et la mortalité liées au cancer.
- * La cascade métastatique implique l'invasion des cellules cancéreuses dans les vaisseaux sanguins ou lymphatiques.
- * Les cellules cancéreuses peuvent rester dormantes pendant des décennies avant de se réactiver.
- * Les mécanismes génétiques et non génétiques sous-tendent l'invasion et la métastase, avec des mutations dans des gènes comme TP53 souvent associées aux lésions métastatiques.
- * Les microenvironnements favorables dans certains organes soutiennent la croissance des métastases.
- * La plasticité phénotypique et les signaux paracrines des cellules du TME influencent l'adaptation métastatique.
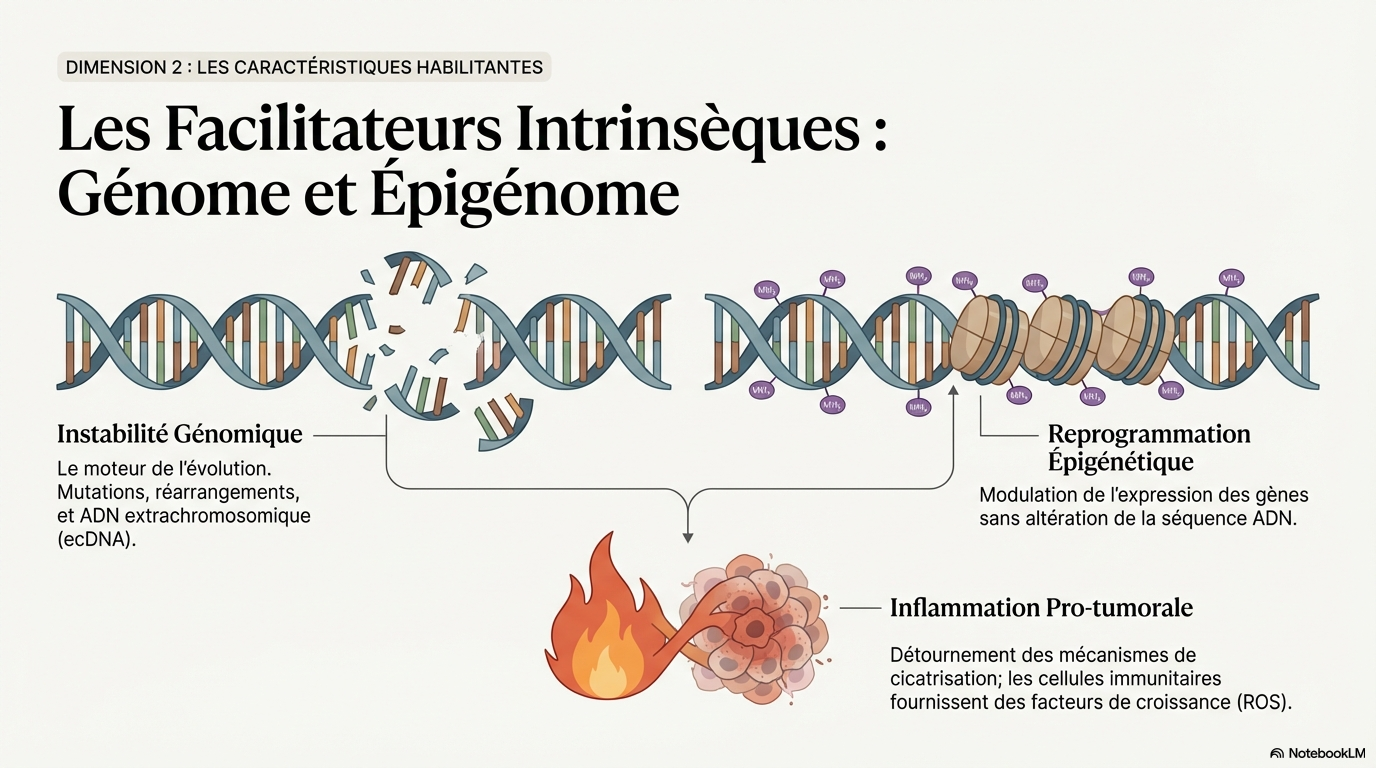
Caractéristiques phénotypiques facilitantes
* Les caractéristiques phénotypiques aberrantes contribuent à l'acquisition des capacités des hallmarks du cancer.
- * La perte de l'intégrité génomique, y compris les mutations et l'instabilité chromosomique (CIN), est fondamentale pour la progression du cancer.
- * La reprogrammation épigénétique non mutatoire joue un rôle crucial dans l'expression des gènes associés aux hallmarks.
- * L'inflammation tumorale favorise la progression tumorale en stimulant des capacités comme la signalisation proliférative et l'évasion immunitaire.
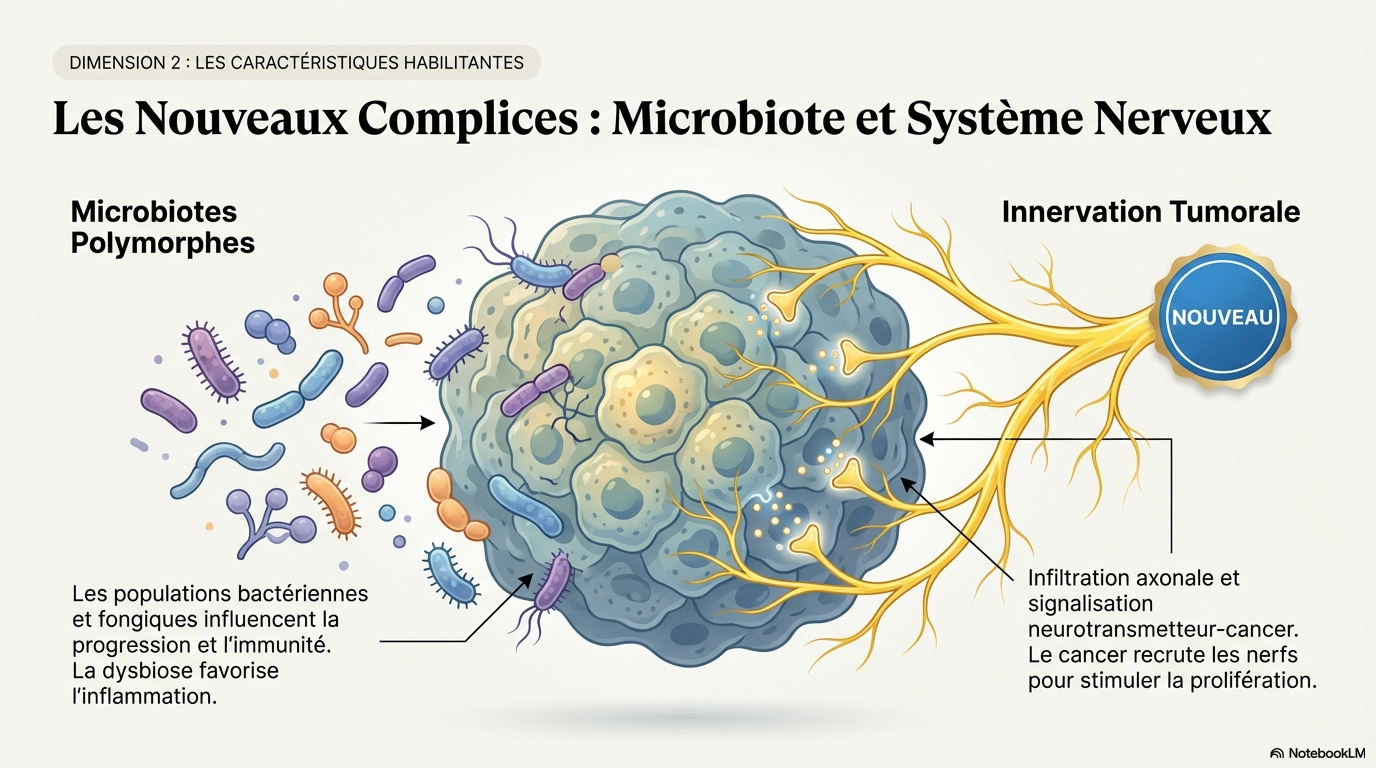
- * L'innervation des tumeurs influence également les capacités cancéreuses, en modulant divers phénotypes.
- * Les microbiomes polymorphes peuvent avoir des effets antagonistes ou protagonistes sur la progression tumorale.
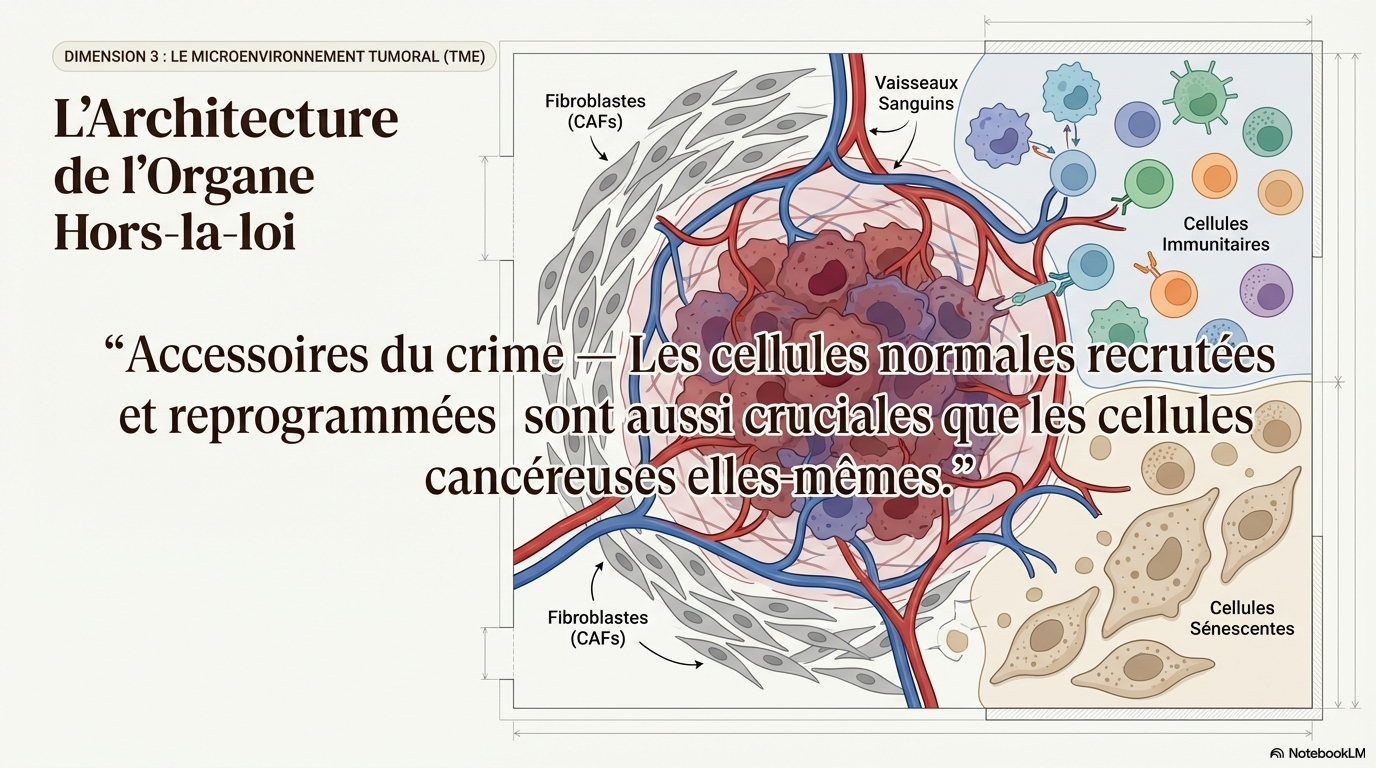
Rôle des cellules dans le microenvironnement tumoral
Les cellules accessoires dans le TME sont essentielles pour manifester les capacités cancéreuses.
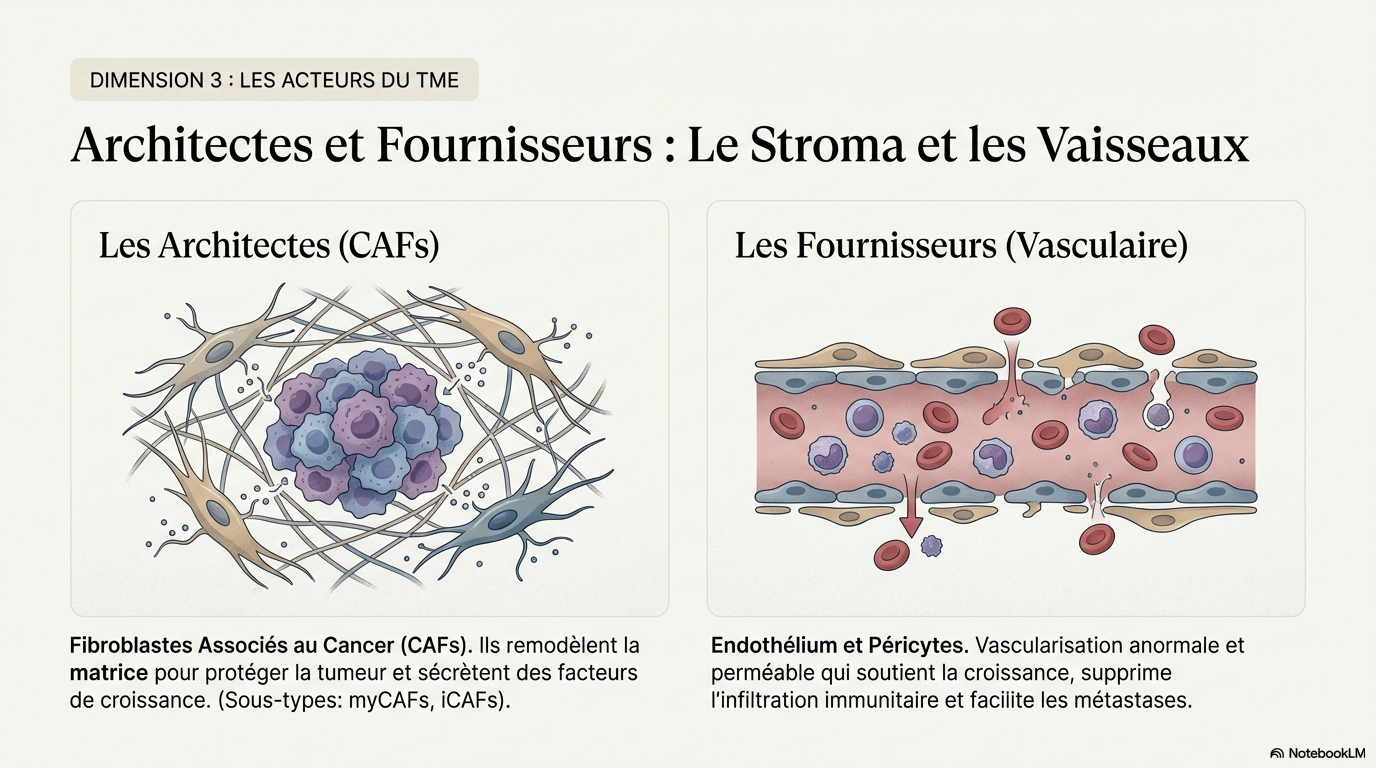
- * Les cellules cancéreuses, les fibroblastes associés aux cancers (CAFs), et les cellules endothéliales contribuent à la progression tumorale.
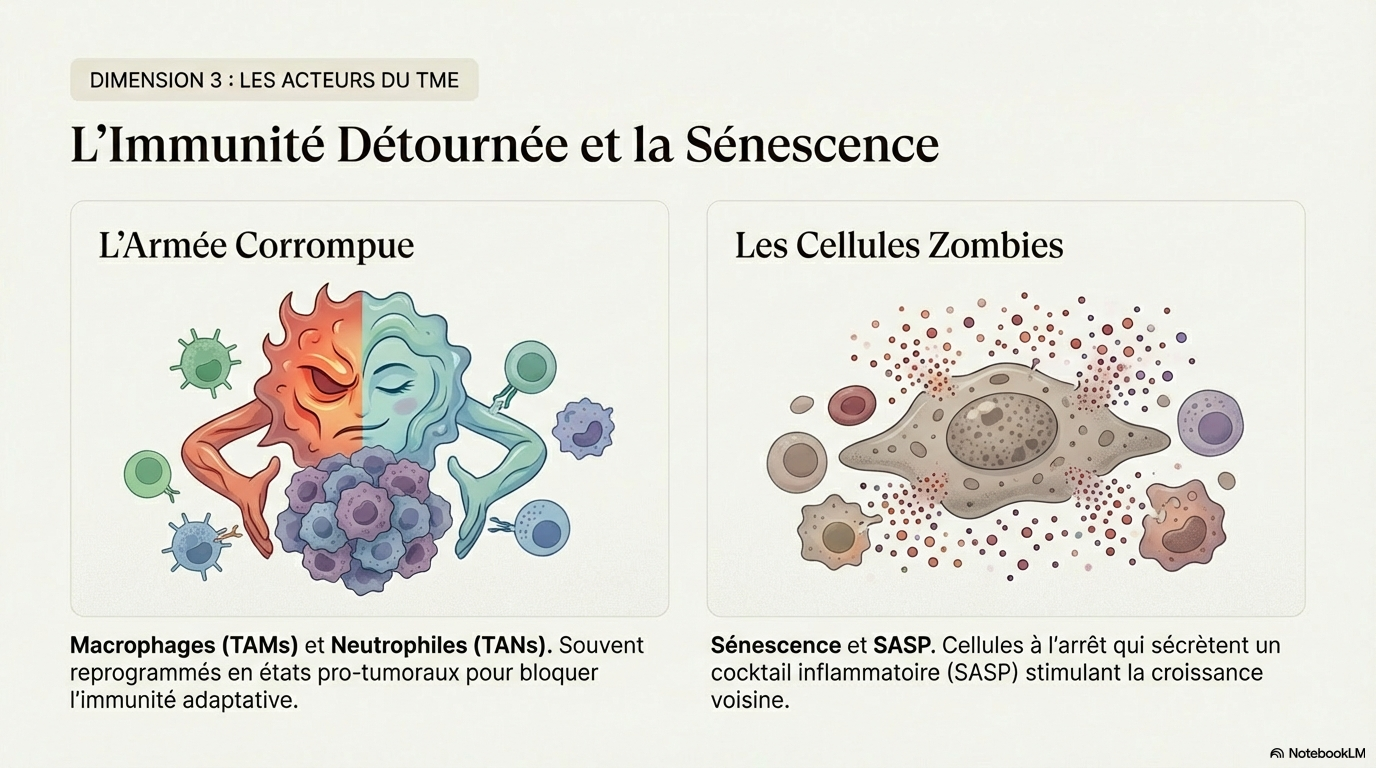
- * Les macrophages et les neutrophiles peuvent adopter des états phénotypiques favorables ou défavorables à la tumeur.
- * cellules sénescentes peuvent moduler la tumorigenèse par leur programme sécrétoire.
- * Les neurones et leurs projections influencent les capacités cancéreuses par des signaux paracrines.
- * Les cellules immunitaires, y compris les Tregs, jouent un rôle dans l'évasion immunitaire.
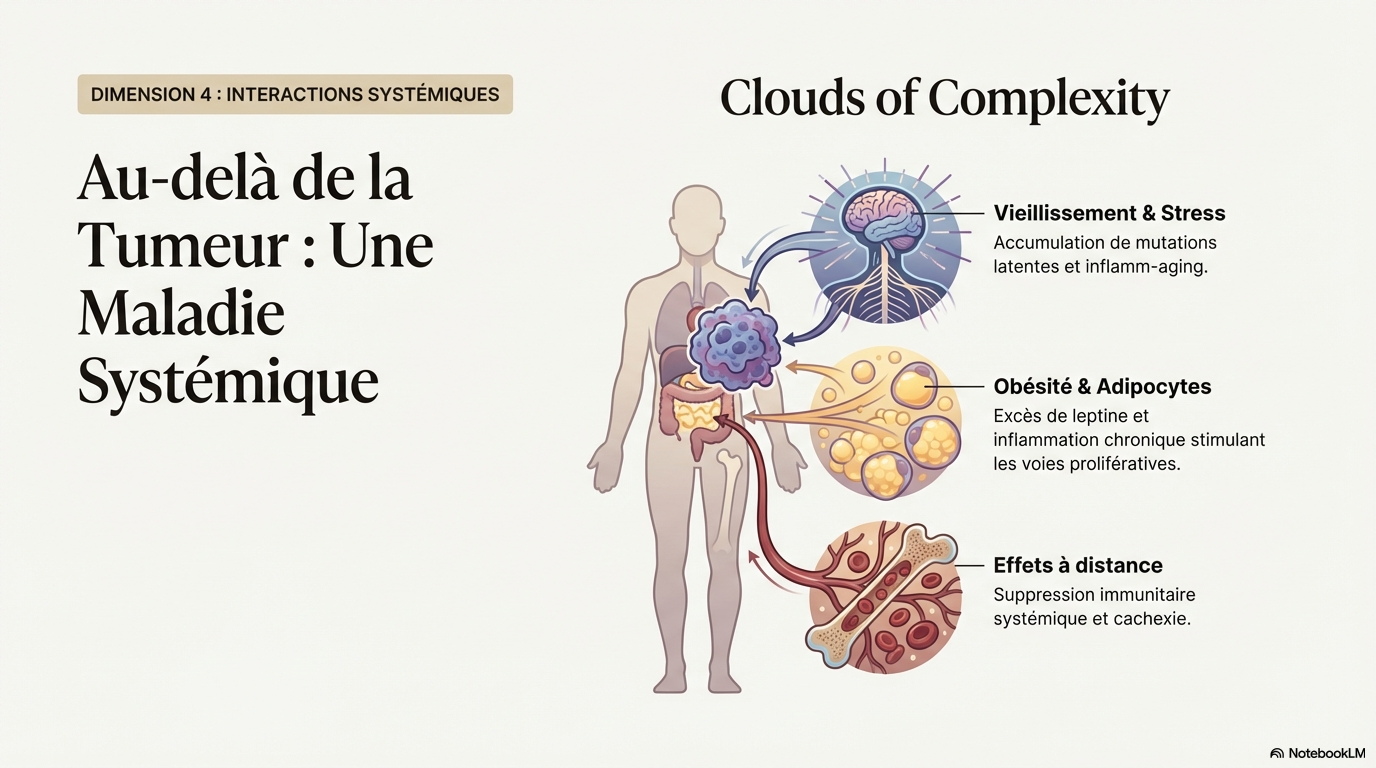
Interactions du cancer comme maladie systémique
Le cancer est une maladie systémique interconnectée avec divers facteurs corporels.
- * Le vieillissement et l'obésité sont des facteurs qui influencent la progression du cancer.
- * Le vieillissement entraîne une accumulation de mutations oncogéniques et une plasticité accrue des cellules.
- * L'obésité est associée à des effets endocriniens qui favorisent la prolifération des cellules cancéreuses et l'inflammation tumorale.
- * Les interactions entre les tumeurs et les systèmes corporels, y compris le microbiome, sont complexes et influencent les capacités cancéreuses.
Perspectives futures sur le cancer
Les recherches futures visent à affiner la compréhension des hallmarks du cancer et à améliorer les traitements.
- * Le profilage multi-omique et l'imagerie non invasive des tumeurs sont des domaines prometteurs pour mieux comprendre la variabilité tumorale.
- * La co-ciblage des capacités des hallmarks pourrait améliorer l'efficacité des traitements contre le cancer.
- * Des stratégies de traitement combinées pourraient réduire le développement de résistances adaptatives aux thérapies.
Stratégies de co-ciblage thérapeutique
Les combinaisons de traitements ciblant les hallmarks du cancer montrent un potentiel prometteur pour améliorer l'efficacité des thérapies anticancéreuses.
- Les inhibiteurs VEGF/VEGFR améliorent la vascularisation tumorale et facilitent l'extravasation des cellules T.
- * Les combinaisons d'inhibiteurs VEGF/VEGFR et d'inhibiteurs de points de contrôle immunitaire (ICIs) ont montré une meilleure efficacité que les monothérapies dans des essais cliniques avancés.
- * Des anticorps monoclonaux bispécifiques anti-VEGFA/PD1 sont en cours d'évaluation, bien qu'aucun n'ait encore reçu l'approbation de la FDA.
- * L'association de l'anticorps anti-VEGFA (bevacizumab) avec l'inhibiteur PARP (olaparib) a conduit à des approbations cliniques pour le cancer de l'ovaire.
Résistance aux thérapies immunitaires
La résistance intrinsèque et adaptative aux immunothérapies est un défi majeur dans le traitement des tumeurs solides.
- * De nombreux types de tumeurs ne répondent pas aux ICIs ou montrent des réponses transitoires.
- La présence de cellules immunosuppressives dans le microenvironnement tumoral contribue à cette résistance.
- * Une stratégie logique consiste à bloquer les points de contrôle immunitaires tout en reprogrammant les cellules immunosuppressives dans le microenvironnement tumoral.
Perspectives futures pour le traitement du cancer
L'avenir des thérapies anticancéreuses repose sur des conceptions de traitement plus sophistiquées et des combinaisons de médicaments.
- * L'exploration des mécanismes de résistance adaptative pourrait prolonger l'efficacité des traitements.
- * Le co-ciblage des mécanismes sous-jacents à des paramètres quasi-indépendants pourrait aboutir à des réponses thérapeutiques plus durables.
- La recherche continue sur les caractéristiques fonctionnelles et les cellules facilitatrices dans le microenvironnement tumoral est essentielle pour développer de nouvelles stratégies thérapeutiques.
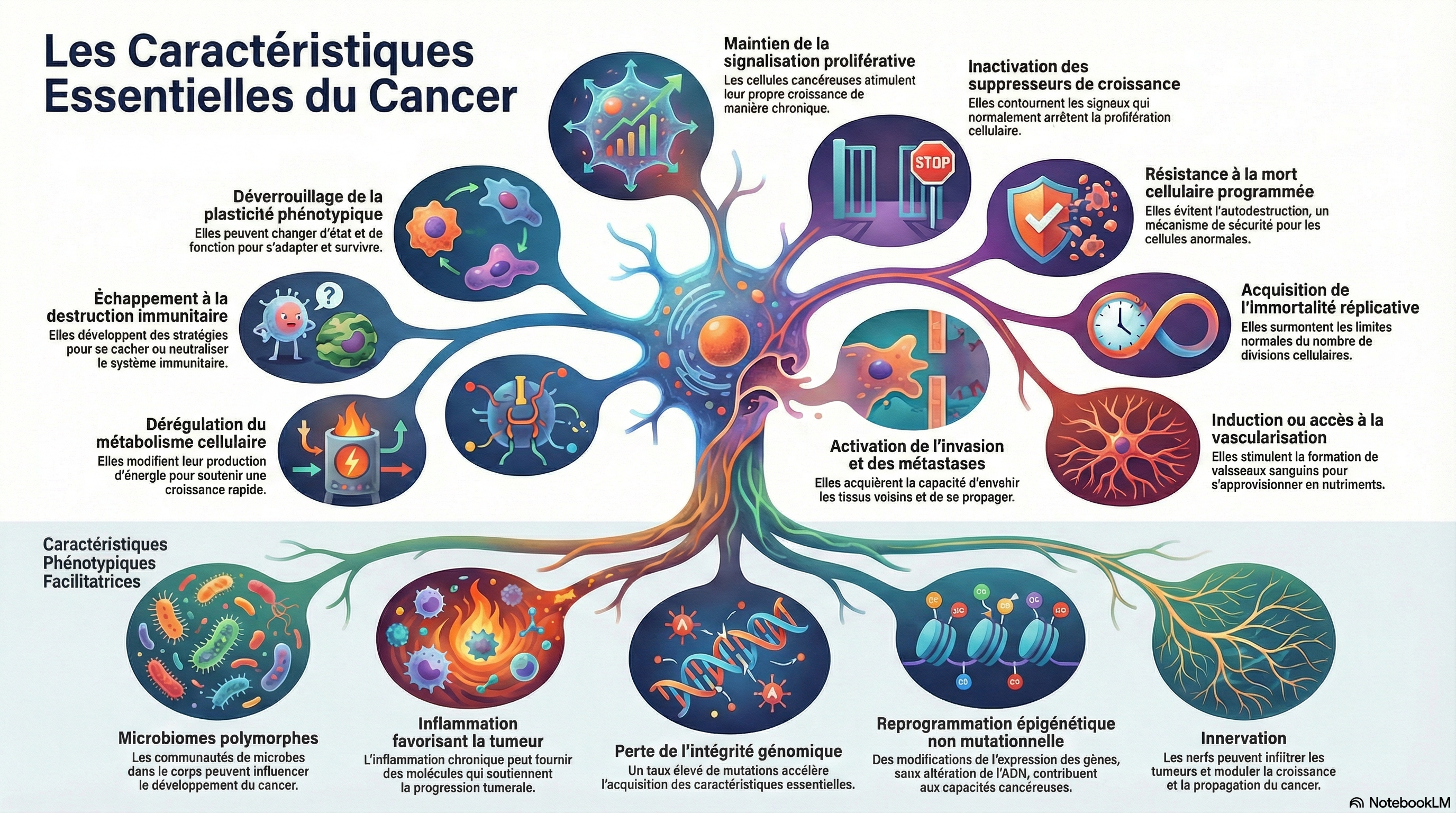
Quels sont les nouveaux piliers du cancer identifiés récemment ?
En résumé, la vision actuelle intègre désormais 9 capacités fonctionnelles (les hallmarks proprement dits) et 5 caractéristiques favorisantes (dont l'épigénétique, le microbiome et l'innervation sont les plus récents), le tout opérant au sein d'un écosystème complexe incluant le microenvironnement tumoral et les interactions systémiques (comme le vieillissement et l'obésité)
DIAPORAMA/NOTEBOOKLM

Commentaire
FEICITATIONS à l'auteur .
A LIRE
https://cancer.ca/fr/get involved/partnerships/chum#:~:text=Le%20potentiel%20de%20l'IA,chances%20de%20sauver%20des%20vies.
Nos projets d'intelligence artificielle contre le cancer et de big data
https://www.centreleonberard.fr/institution/ce-que-nous-sommes/innover-intelligence-artificielle-cancerologie
IA en oncologie: "Le potentiel est énorme mais l'enjeu maintenant, c'est la qualité, pas la quantité"
https://www.vidal.fr/actualites/37123-ia-en-oncologie-le-potentiel-est-enorme-mais-l-enjeu-maintenant-c-est-la-qualite-pas-la-quantite.html



